Obesità, microbiota e parodontite: un’unica storia infiammatoria
Ernesto Bruschi — bonebenders.com
Sommario / Summary
IT — Questo articolo esplora le connessioni tra obesità, microbiota orale e intestinale, metabolismo del glucosio e parodontite. L’asse bocca-intestino, il pathway del GLP-1 e l’infiammazione cronica di basso grado formano un triangolo patologico che il clinico deve conoscere e saper interrompere.
EN — This article explores the connections between obesity, oral and gut microbiota, glucose metabolism, and periodontal disease. The oral-gut axis, the GLP-1 pathway, and chronic low-grade inflammation form a pathological triangle that clinicians must understand and learn to disrupt.
La medicina, quella vera, che non è fatta di egoismi, di prepotenze e di sbandieramento di titoli, è un percorso di vita. È riconoscersi nei timori e nelle speranze del prossimo. È ricerca costante. È curiosità inesauribile per la fisiologia, la patologia e la farmacologia.
Un titolo universitario, una specializzazione, un corso di aggiornamento sono tutte ottime basi di partenza. Ma poi tocca a ognuno di noi cercare la conoscenza. Dobbiamo applicarci tutti i giorni per tentare di migliorarci per i nostri pazienti e per noi stessi.
Una delle cose che ho imparato, forse più nel corso del tempo, è che la medicina a compartimenti stagni è una bufala. Non esiste. Nel nostro campo, i denti e la bocca, i collegamenti fisiopatologici con gli altri organi sono qualcosa che viviamo quotidianamente.
E poi ci sono i delicatissimi equilibri che collegano la bocca, un ambiente molto intimo, alla sfera psichica.
E, talvolta, questi collegamenti tra compartimenti anatomici molto diversi mi sorprendono ancora.
È il caso dell’intricata relazione, che cercherò di descrivere al meglio delle mie possibilità in questo articolo, che coinvolge, oltre la parodontologia, anche la diabetologia, e la gastroenterologia. Non molti lo cercano. Eppure il filo esiste, ed è fatto di batteri, di citochine e di un ormone chiamato Glucagon-Like Peptide-1 (GLP-1).
Il microbiota intestinale nell’obesità
Il primo nodo è nell’intestino.
Il paziente obeso ha microflora intestinale alterata. La diversità batterica è ridotta, la quota di Firmicutes cresce a spese dei Bacteroidetes, e i batteri produttori di acidi grassi a catena corta — i SCFA (Short Chain Fatty Acids), acetato, propionato, butirrato — calano in numero e in attività.
Sono i prodotti della fermentazione batterica delle fibre (la quota indigeribile) nel colon. Nutrono le cellule intestinali, riducono l’infiammazione e migliorano la salute metabolica. Il butirrato è la fonte energetica primaria per le cellule del colon (colonciti) e aiuta a rinforzare la barriera intestinale.
Se il butirrato è ridotto, potenzialmente aumenta la permeabilità delle “tight junctions” e si verifica il fenomeno detto “leaky gut”: un’elevata quantità di tossine è raccolta dalla vena porta e raggiunge il fegato. I lipopolisaccaridi batterici (LPS) entrano nel circolo portale. È l’endotossemia metabolica: un flusso continuo e sottosoglia di tossine batteriche che attivano i recettori TLR4 e mantengono acceso il fuoco del TNF-α, dell’IL-6, dell’IL-1β. Questi meccanismi alimentano un’infiammazione cronica di basso grado che agisce in silenzio, per anni. Insulina e recettori per l’insulina lavorano in un ambiente sempre più ostile. La resistenza insulinica avanza.
Questi fenomeni, se persistenti nel tempo, possono generare una steatosi, e una cirrosi epatica.
Un’alimentazione ricca di fibre ha un effetto benefico perché aumenta la produzione di SCFA e alimenta le cellule intestinali. Gli SCFA, inoltre, aiutano la motilità intestinale e hanno proprietà antiossidanti.
Allo stesso tempo, se si assumono troppe fibre improvvisamente, si verifica fermentazione eccessiva e il noto fenomeno del gonfiore e della flatulenza. Sono sempre gli SCFA a provocarla, unitamente ad altri sottoprodotti. Per ridurre la flatulenza, si consiglia di aumentare il consumo di fibre gradualmente, permettendo al microbiota di adattarsi in modo progressivo senza eccessiva produzione di gas.
Un capitolo recente — e clinicamente sottovalutato — riguarda l’obesità sarcopenica. In questa condizione, l’accumulo di grasso viscerale è accompagnato da perdita di massa muscolare. Il microbiota dismicrobico è uno dei meccanismi centrali di tale patologia perché interferisce con la segnalazione anabolica e con la regolazione ormonale.
L’asse bocca-intestino
Il secondo nodo è in bocca.
La parodontite è una malattia sistemica. Oggi sappiamo che è anche una malattia dell’asse orale-intestinale. La via è semplice: ogni giorno ingoiamo saliva. Ogni giorno, in un paziente con parodontite attiva, quella saliva trasporta Porphyromonas gingivalis, Fusobacterium nucleatum, Treponema denticola verso l’intestino. Lì, questi patogeni non restano spettatori. Colonizzano anche l’intestino e alterano la composizione del microbiota locale. Aumentano la permeabilità intestinale delle “tight junctions”, e attivano risposte immunologiche scompensanti che si sovrappongono a quelle già in corso.
Le vescicole extracellulari batteriche (BEV) fanno il resto: attraversano le barriere mucosali e agiscono a distanza come mediatori infiammatori transbarriera. Anche se non entrano direttamente in circolo, questi batteri sono capaci di indurre un danno sistemico.
Una recente review pubblicata sul Journal of Crohn’s & Colitis (Tanwar et al., 2024) ha formalizzato il concetto di “gum-gut axis” (asse gengiva-intestino), documentando la prevalenza reciprocamente aumentata di parodontite nei pazienti con malattia infiammatoria intestinale e viceversa.
Il modello proposto è quello del “multi-hit”: eventi successivi e continuativi che si sommano nel tempo. Ciascun evento singolo (come una massiva carica batterica parodontale che raggiunge le pareti intestinali) è insufficiente da solo. Ma quando tali eventi si ripetono in modo persistente, sarebbero letali per l’omeostasi del microbiota intestinale.
Perché alcuni batteri orali sopravvivono all’acido gastrico?
Lo stomaco non è una camera sterile a pH costante. Il pH varia da 1,5–2 a digiuno fino a 4–6 durante e dopo il pasto, quando la presenza del cibo riduce l’acidità. La finestra post-prandiale è la porta di ingresso principale per i batteri orali — deglutiti in grandi quantità con saliva e cibo, arrivano in un ambiente transitoriamente meno ostile.
Alcuni batteri hanno inoltre meccanismi intrinseci di resistenza all’acido: pompe protoniche, sistemi tampone intracellulari, produzione di ammonio (classico esempio: Fusobacterium nucleatum e alcuni streptococchi orali).
Con ogni deglutizione transitano circa 10⁸ batteri orali. Se anche solo lo 0,01% sopravvive, arrivano all’intestino 10⁴ cellule per deglutizione — moltiplicate per le migliaia di deglutizioni quotidiane. La pressione numerica è enorme.
Fusobacterium nucleatum (un parodonto-patogeno classico) è il caso più studiato in quanto ritrovato in abbondanza nel tessuto tumorale colorettale. Porphyromonas gingivalis, Treponema denticola, Peptostreptococcus — altri parodonto-patogeni — sono stati identificati in campioni di mucosa intestinale infiammata.
Microbiota intestinale, GLP-1 e glucosio
Il terzo nodo è il più sottile, ed è quello che dovrebbe interessarci di più come clinici.
I SCFA prodotti dalla fermentazione batterica delle fibre alimentari indigeribili attivano i recettori accoppiati a proteine G — GPR43 e GPR41 — sulle cellule L intestinali. Quella attivazione stimola la secrezione di GLP-1, che a sua volta potenzia la secrezione insulinica glucosio-dipendente, rallenta lo svuotamento gastrico, riduce l’appetito, protegge le cellule beta del pancreas. È il meccanismo che spiega perché la presenza di popolazioni adeguate di Lachnospiraceae, Akkermansia muciniphila e Faecalibacterium prausnitzii — i principali batteri intestinali produttori di butirrato — difende dal rischio di diabete tipo 2.

Nell’obeso (anche nel sovrappeso) e nel diabetico queste specie batteriche sono ridotte. Meno SCFA, meno GLP-1, più iperglicemia postprandiale, più resistenza all’insulina. Il ciclo si chiude su se stesso.
Ma c’è probabilmente un importante effetto di ritorno.
Uno studio condotto sul modello murino (Sawada et al., 2020, Journal of Diabetes Research) ha evidenziato che il liraglutide (Saxenda o Victoza), ha un effetto protettivo sui tessuti parodontali. La liraglutide è un analogo del GLP-1, non un farmaco che agisce sui suoi livelli endogeni. La distinzione è importante.
La liraglutide è una molecola sintetica strutturalmente analoga al GLP-1 umano, con il 97% di omologia. La modifica chiave è l’aggiunta di una parte che la lega all’albumina plasmatica, proteggendola dalla degradazione enzimatica e prolungandone l’emivita a circa 13 ore, sufficiente per una somministrazione giornaliera. La molecola naturale, al contrario, si degrada nel giro di pochi minuti.
Questo farmaco, in aggiunta agli effetti metabolici, riduce l’infiltrazione infiammatoria a livello gengivale, diminuisce la presenza di macrofagi M1 e attenua il riassorbimento osseo alveolare indotto dalla parodontite sperimentale. È evidente che il GLP-1 umano avrà caratteristiche protettive analoghe.
Cosa fa concretamente per il paziente dismetabolico
Agisce sugli stessi recettori del GLP-1 endogeno (GLP-1R), con effetti sovrapponibili ma prolungati: stimola la secrezione insulinica in modo glucosio-dipendente, sopprime il glucagone, rallenta lo svuotamento gastrico, riduce l’appetito agendo sui centri ipotalamici della sazietà.
Semaglutide: analogo del GLP-1 di seconda generazione
Come la liraglutide, è un analogo strutturale del GLP-1 umano — omologia del 94%. Agisce sugli stessi recettori (GLP-1R) con gli stessi effetti: secrezione insulinica glucosio-dipendente, soppressione del glucagone, rallentamento dello svuotamento gastrico, riduzione dell’appetito a livello ipotalamico.

Cosa la distingue dalla liraglutide
La modifica chimica è più sofisticata e la lega all’albumina con maggiore affinità. Il risultato è un’emivita di circa 165–170 ore. Questo permette la somministrazione settimanale (Ozempic per il diabete, Wegovy per l’obesità) o addirittura mensile nelle formulazioni orali (Rybelsus, unico GLP-1 disponibile per via orale).
Efficacia sul peso
Superiore alla liraglutide. Negli studi STEP, semaglutide 2,4 mg/settimana ha prodotto una riduzione media del peso corporeo del 15–17% a 68 settimane, contro il 5–8% della liraglutide 3 mg/die. La differenza è probabilmente legata alla maggiore penetrazione a livello del sistema nervoso centrale e a una soppressione dell’appetito più prolungata e intensa.
Rilevanza per il tuo contesto clinico
Pazienti obesi o in sovrappeso viscerale trattati con semaglutide mostrano riduzioni significative di PCR, IL-6 e altri marcatori infiammatori — indipendentemente dal calo ponderale. Un paziente parodontopatico in terapia con semaglutide sta quindi modificando anche il substrato infiammatorio sistemico che alimenta la malattia parodontale. Vale la pena tenerlo in conto nella valutazione della risposta alla terapia.
Il triangolo che si chiude
Obesità, parodontite e diabete tipo 2 condividono tre meccanismi fondamentali.
Il primo è l’infiammazione cronica di basso grado. Il tessuto adiposo viscerale secerne adipochine proinfiammatorie. Il tessuto parodontale malato libera IL-1β, IL-6, TNF-α nel circolo sistemico. Le due fonti si sommano: il carico infiammatorio complessivo supera la capacità tampone dell’organismo e le due condizioni patologiche si alimentano in modo esponenziale.
Il secondo è la resistenza insulinica. Le citochine infiammatorie interferiscono con la cascata di segnalazione dell’insulina a livello recettoriale e post-recettoriale. La direzione è bidirezionale: il parodonto malato peggiora il diabete, il diabete peggiora la parodontite.
Il terzo è la disbiosi microbica — orale e intestinale — come causa e come conseguenza. Non si tratta di due compartimenti separati ma di un continuum microbico che il clinico deve imparare a leggere come tale.

Il punto cruciale è questo: trattare la parodontite riduce i marcatori infiammatori sistemici e migliora il controllo glicemico. L’effetto non è drammatico, ma è reale, documentato, ripetibile. Il parodontologo deve raccogliere un’anamnesi accurata e accertarsi che i livelli glicemici siano monitorati dal paziente e dal medico che lo segue.
Ma chi è “l’obeso”?
Un individuo è definito obeso quando l’indice di massa corporea (BMI) supera i 30 kg/m². Il BMI (Body Mass Index) o IMC (Indice di Massa Corporea) si calcola dividendo il peso corporeo in kg per il quadrato dell’altezza in metri (BMI=peso(KG)/altezza(m)2.
Nel normopeso (BMI 18,5–24,9) il rischio metabolico e cardiovascolare è più basso, a parità di condizioni, rispetto alle persone con indice più elevato.
Anche la condizione di sovrappeso (BMI 25–29,9), come, per esempio, un uomo di 175 cm che pesa tra 78 e 92 kg non è una condizione neutra. Il rischio di diabete tipo 2 inizia ad aumentare già a partire da BMI 25. Si osservano incrementi della pressione arteriosa, i primi segni di insulino-resistenza, aumento dei trigliceridi. In presenza di grasso viscerale prevalente — misurato dalla circonferenza vita — il profilo di rischio si avvicina a quello della classe I di obesità. Il sovrappeso è la categoria più popolosa nelle società occidentali e quella più sottovalutata clinicamente, proprio perché i valori di laboratorio restano spesso nei limiti per anni, mascherando un deterioramento metabolico silente ma progressivo.
Obesità Classe I (BMI 30–34,9). Un uomo di 175 cm che pesa tra 92 e 107 kg. Rischio aumentato di diabete tipo 2, ipertensione, dislipidemia.
Obesità Classe II (BMI 35–39,9). Stessa altezza, peso tra 107 e 122 kg. Rischio elevato. Spesso presenti già una o più comorbidità.
Obesità Classe III, grave (BMI ≥ 40). Stessa altezza, peso 122 kg e oltre. Rischio molto elevato. Compromissione funzionale frequente — apnee notturne, difficoltà deambulatoria, reflusso grave.

Rilevanza in ambito odontoiatrico
L’obesità, specie viscerale, è associata a uno stato infiammatorio sistemico cronico di basso grado — elevati livelli di IL-6, TNF-α, proteina C-reattiva. Questo ambiente pro-infiammatorio favorisce, a cascata, anche la progressione della parodontite e può compromettere la guarigione peri-implantare. Vale la pena notare che il rischio non compare bruscamente a BMI 30: studi recenti suggeriscono un’associazione significativa anche tra il semplice sovrappeso e la parodontite già nella fascia 25–29,9, proporzionale all’entità del grasso viscerale.
Il paziente in sovrappeso con parodontite non va sottovalutato. Il paziente obeso con parodontite grave non è un caso raro: è una combinazione che si autoalimenta.
È un po’ come il fumatore incallito. A un certo punto le condizioni si sovrappongono e si autoalimentano tra loro. Ripari da una parte della bocca e succede qualcosa di nuovo dall’altra. Ed è per questo che guarire dall’obesità (e smettere di fumare) è una situazione “win-win” per il paziente parodontale e per il dentista che lo cura.
Conclusione
La bocca non è un’isola deserta in mezzo all’oceano.
I dati ci dicono che l’infiammazione parodontale parla con l’intestino, l’intestino parla con il pancreas, il pancreas con il tessuto adiposo. Il circuito è chiuso e si autoalimenta. Spezzarlo richiede di entrare nella patologia da più punti contemporaneamente.
Il parodontologo e il dentista possono influire su uno di questi ambienti, la bocca. Impegnarsi per proteggere il paziente è una missione fondamentale e un dovere professionale. Collaborare con altri specialisti per una terapia integrata volta al benessere del paziente è molto importante.
Una cura metabolica può anche partire, inizialmente, dal nostro indirizzare il paziente bisognoso verso altri medici. Certamente, poi saranno gli altri specialisti a portarla avanti con le loro competenze specifiche. Ma l’obiettivo è salvare il paziente. E richiede impegno.
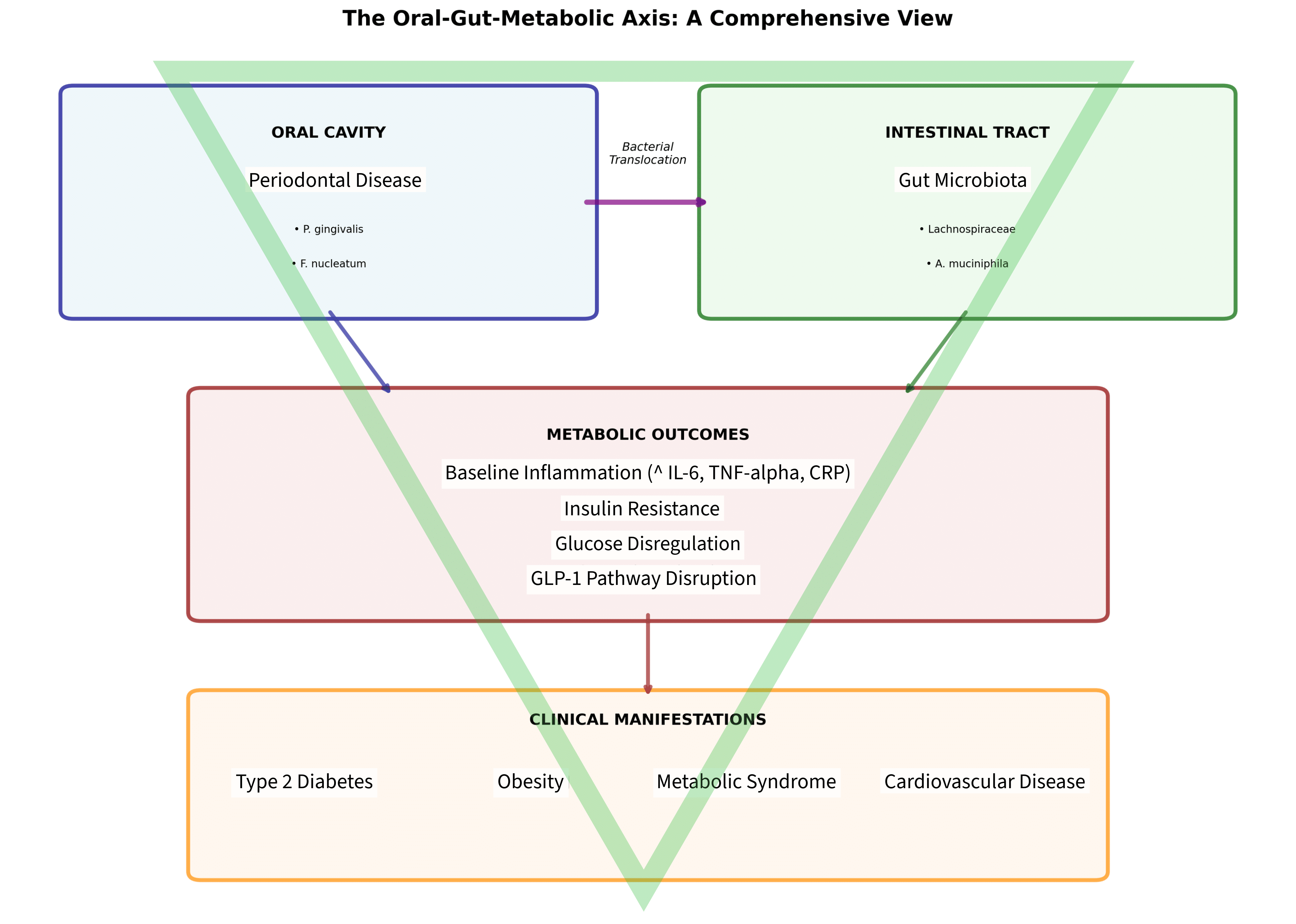
L’immagine che segue riassume i percorsi fisiopatologici descritti nel presente articolo:

La prossima volta che curate un paziente odontoiatrico, calcolate il BMI. Curatelo e indirizzatelo agli altri specialisti per le cure del caso.
Ausili terapeutici
Probiotici e microbiota. Le evidenze sull’uso di probiotici nel trattamento parodontale (in particolare Lactobacillus reuteri) sono in crescita. Non sono ancora terapia di prima linea, ma il razionale biologico è solido e i trial clinici si moltiplicano.
Farmaci sistemici come alleati. Gli analoghi del recettore GLP-1 — semaglutide, liraglutide — hanno effetti antinfiammatori documentati che vanno oltre la riduzione glicemica. In un paziente diabetico con parodontite severa, la scelta del farmaco ipoglicemizzante non è indifferente.
Riferimenti
- Tanwar H et al. Unravelling the Oral-Gut Axis: Interconnection Between Periodontitis and Inflammatory Bowel Disease. J Crohns Colitis. 2024;18(8):1319-1341. https://doi.org/10.1093/ecco-jcc/jjae028
- Shinjo T, Nishimura F. The bidirectional association between diabetes and periodontitis, from basic to clinical. Jpn Dent Sci Rev. 2023;60:15-21. https://doi.org/10.1016/j.jdsr.2023.12.002
- Kuraji R et al. Periodontal treatment and microbiome-targeted therapy in management of periodontitis-related nonalcoholic fatty liver disease with oral and gut dysbiosis. World J Gastroenterol. 2023;29(6):967-996. https://doi.org/10.3748/wjg.v29.i6.967
- Sawada N et al. Glucagon-Like Peptide-1 Receptor Agonist Liraglutide Ameliorates the Development of Periodontitis. J Diabetes Res. 2020;2020:8843310. https://doi.org/10.1155/2020/8843310
- Harrandah AM. The Oral-Gut-Systemic Axis: Emerging Insights into Periodontitis, Microbiota Dysbiosis, and Systemic Disease Interplay. Diagnostics (Basel). 2025;15(21). https://doi.org/10.3390/diagnostics15212784
- Baima G et al. Periodontitis and risk of cancer: Mechanistic evidence. Periodontol 2000. 2024;96(1):83-94. https://doi.org/10.1111/prd.12540
- Lebrun, L. J., Lenaerts, K., Kiers, D., Pais de Barros, J. P., Le Guern, N., Plesnik, J., Thomas, C., Bourgeois, T., Dejong, C. H. C., Kox, M., Hundscheid, I. H. R., Khan, N. A., Mandard, S., Deckert, V., Pickkers, P., Drucker, D. J., Lagrost, L., & Grober, J. (2017). Enteroendocrine L Cells Sense LPS after Gut Barrier Injury to Enhance GLP-1 Secretion. Cell reports, 21(5), 1160–1168. https://doi.org/10.1016/j.celrep.2017.10.008
FAQ:
Qual è il collegamento tra obesità, microbiota intestinale e parodontite?
L’obesità altera la microflora intestinale, riducendo la diversità batterica e i produttori di acidi grassi a catena corta, favorendo un’infiammazione cronica di basso grado che può aggravare la parodontite. Questa condizione crea un ciclo infiammatorio che coinvolge anche altri organi.
Come influisce la parodontite sulla salute intestinale e viceversa?
La saliva contenente batteri come Porphyromonas gingivalis e Fusobacterium nucleatum può essere ingoiata e colonizzare l’intestino, alterando il microbiota locale e aumentando la permeabilità intestinale, contribuendo a risposte infiammatorie sistemiche e peggiorando condizioni come la malattia infiammatoria intestinale.
Che ruolo ha il microbiota intestinale nel controllo del diabete di tipo 2?
Il microbiota intestinale produce SCFA che stimolano il rilascio di GLP-1, un ormone che aumenta la secrezione insulinica e riduce l’appetito. Quando questo meccanismo è alterato, si può sviluppare resistenza all’insulina e diabete di tipo 2.
In che modo i farmaci come la liraglutide e la semaglutide aiutano nei casi di obesità e parodontite?
Questi farmaci, analoghi del GLP-1, stimolano la secrezione di insulina, riducono l’infiammazione gengivale e diminuiscono la perdita ossea causata dalla parodontite, migliorando anche i parametri infiammatori sistemici e favorendo la perdita di peso.
Perché è importante che il dentista consideri il BMI del paziente?
Il BMI è importante perché l’obesità, specialmente quella viscerale, è associata a uno stato infiammatorio sistemico che può aggravare le malattie parodontali; valutare e monitorare il BMI aiuta a pianificare trattamenti più efficaci e a indirizzare il paziente verso altri specialisti per un intervento integrato.