Treponema denticola: la spirocheta del complesso rosso
Read in English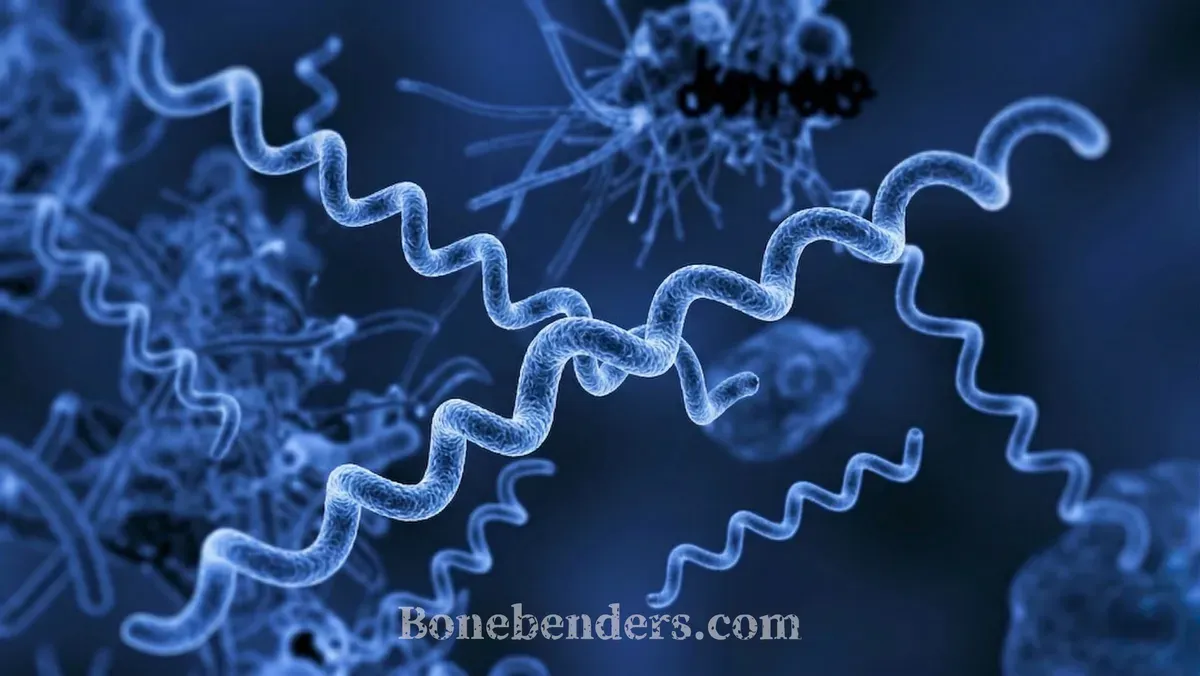
In breve — Treponema denticola è una spirocheta orale anaerobia del complesso rosso di Socransky. Si distingue dagli altri patogeni parodontali per la sua motilità: flagelli periplasmatici che le consentono di penetrare tessuti dove i batteri immobili non arrivano. Possiede una proteasi di superficie, la dentilisina, che degrada le difese dell’ospite e facilita la coaggregazione con gli altri membri del complesso rosso. Studi recenti la collegano anche a malattie neurodegenerative.
Summary (EN) — Treponema denticola is an anaerobic oral spirochete belonging to Socransky’s red complex. Its periplasmic flagella allow tissue penetration; its surface protease dentilisin degrades host defenses and enables coaggregation with P. gingivalis and T. forsythia. Emerging evidence links it to neurodegenerative diseases.
Nel complesso rosso di Socransky, ogni membro ha un ruolo. Porphyromonas gingivalis è il regista: orchestra la disbiosi, sovverte le difese, rimodella l’ambiente. Tannerella forsythia è il complice silenzioso, presente ovunque il danno sia già stato fatto.
Treponema denticola è un’altra cosa. È quello che si muove. Immaginate una specie di micro-serpente che si muove, “avvitandosi” nel biofilm della tasca gengivale.
Una forma antica
Le spirochete sono tra i batteri più antichi del pianeta. La loro forma elicoidale non è un caso: è una soluzione ingegneristica. Mentre la maggior parte dei batteri nuota in fluidi liberi grazie a flagelli esterni, le spirochete hanno risolto un problema diverso — muoversi attraverso ambienti viscosi, densi, semisolidi.
T. denticola ha una struttura a tre strati. Al centro il cilindro protoplasmatico, che contiene il patrimonio genetico e la macchina metabolica. Attorno, nello spazio periplasmatico, corrono i flagelli — detti flagelli periplasmatici o endoflagelli. All’esterno, una guaina (outer sheath) che avvolge tutto come una membrana elastica.
I flagelli periplasmatici sono il cuore del sistema. Sono ancorati ai poli della cellula e si estendono verso il centro, sovrapponendosi. Quando ruotano, generano un’onda che si propaga lungo l’intero corpo batterico. Il risultato è un movimento a cavatappi che permette alla spirocheta di attraversare il muco, il fluido crevicolare, il tessuto connettivo gengivale. Kurniyati e colleghi hanno dimostrato nel 2022 che il fattore sigma FliA (TDE2683) regola l’espressione dei geni flagellari tardivi e controlla la simmetria dei flagelli: quando è alterato, la motilità crolla.
Questo movimento non è casuale. T. denticola è chemiotattica: si dirige, cioè, verso i nutrienti. Ruby e colleghi hanno mostrato che anche il semplice glucosio induce una risposta chemiotattica motilità-dipendente. Il batterio non vaga a caso: cerca, trova, penetra.
La guaina e le sue armi
La guaina esterna di T. denticola non è un semplice involucro. È una piattaforma armata.
Due proteine dominano la sua superficie.
Msp (major sheath protein) è una porina — una proteina che forma canali nella membrana. Ma Msp fa molto di più: è citotossica per i poveri fibroblasti gengivali, altera la permeabilità delle cellule epiteliali, e contribuisce all’adesione del batterio ai tessuti dell’ospite. Sela, nella sua revisione del 2001 su Critical Reviews in Oral Biology and Medicine, la definì uno dei principali determinanti di virulenza.
Dentilisina è una proteasi di superficie con attività simil-chimotripsina. Degrada proteine della matrice extracellulare — fibronectina, laminina, componenti del complemento — e altera le giunzioni strette (tight junctions) tra le cellule epiteliali, aprendo la strada all’invasione batterica. Ma il suo ruolo non si ferma qui.
Kokubu e colleghi hanno dimostrato nel 2021 che la dentilisina facilita anche il crawling — il movimento strisciante su superfici solide. Ceppi mutanti privi di dentilisina mostravano colonie più piccole e velocità di spostamento ridotta. La proteasi, quindi, non è solo un’arma: è anche un motore di spostamento.
L’alleanza con Porphyromonas gingivalis
Il complesso rosso crea un “consorzio metabolico”.
Zhu e colleghi, nel 2013 su PLoS ONE, hanno documentato una forte sinergia tra P. gingivalis e T. denticola nella formazione di biofilm polimicrobici. In co-coltura, entrambe le specie aumentavano significativamente il biovolume, lo spessore medio e lo spessore massimo del biofilm. Le gingipaìne di P. gingivalis si sono rivelate essenziali per questa sinergia: un P. Gingivalis mutante privo di gingipaìne non era in grado di formare biofilm polimicrobici con T. denticola.
Nel 2020, Kin e colleghi hanno svelato il meccanismo metabolico sottostante, pubblicando su Journal of Oral Microbiology. P. gingivalis idrolizza peptidi contenenti glicina e produce glicina libera, che T. denticola utilizza come fonte primaria di energia e carbonio. In cambio, P. gingivalis riceve succinato. È una cooperazione metabolica vera: i due batteri si spartiscono le risorse, e insieme diventano più efficienti di quanto sarebbero da soli.
Richard Darveau, nel 2010 su Nature Reviews Microbiology, ha descritto la parodontite come una grave alterazione polimicrobica dell’omeostasi dell’ospite. T. denticola è un attore centrale di questo fenomeno. È un forte amplificatore della patogenicità degli altri batteri coinvolti.
La dentilisina gioca un ruolo anche nella coaggregazione con Tannerella forsythia. Sano e colleghi hanno mostrato nel 2014 su Anaerobe che ceppi di T. denticola privi di dentilisina perdevano la capacità di coaggregare con T. forsythia. Non per effetto proteolitico diretto, ma probabilmente attraverso la maturazione di ligandi di superficie. Un meccanismo indiretto, elegante.
Oltre la bocca
Come P. gingivalis, anche T. denticola è sospettata di raggiungere siti distanti dalla cavità orale.
Pisani e colleghi, nel 2023 su International Journal of Environmental Research and Public Health, hanno proposto un’ipotesi suggestiva: T. denticola potrebbe causare neurodegenerazione nel mesencefalo attraverso la via periodonale. La spirocheta è neurotrofica — può viaggiare lungo gli assoni dei nervi periferici del legamento parodontale, raggiungere il locus coeruleus e da lì estendere il danno alla corteccia. I meccanismi ipotizzati includono il danneggiamento citoscheletrico, l’alterazione del trasporto assonale e la disfunzione mitocondriale.
D’altronde il cugino Treponema pallidum, agente infettivo responsabile della sifilide, ha un neurotropismo ben dimostrato e causa la neurolue.
Un dato in più: Mahendrarajan e colleghi nel 2025, su Frontiers in Oral Health, hanno descritto il ruolo delle vescicole di membrana esterna (OMV) dei batteri del complesso rosso — T. denticola incluso — come vettori di virulenza a distanza, capaci di influenzare aterosclerosi, artrite reumatoide e diabete mellito.
Sono ipotesi, non certezze. Ma la direzione della ricerca è chiara: quello che succede nel solco gengivale non resta nel solco gengivale.
Cosa significa per chi cura
T. denticola è un anaerobio obbligato. Vive solo dove l’ossigeno non arriva — nel fondo delle tasche parodontali, nel biofilm subgengivale maturo, negli spazi dove il tessuto è già compromesso. Questo dato, da solo, indica la strategia terapeutica.
La rimozione meccanica del biofilm — scaling, root planing, chirurgia resettiva o rigenerativa quando indicata — è il modo più diretto per ridurne la carica. T. denticola non sopravvive in un solco pulito e poco profondo. Il mantenimento parodontale regolare impedisce la ricolonizzazione.
Dashper e colleghi, nella loro revisione del 2010 su Journal of Dental Research, hanno sottolineato che T. denticola possiede anche determinanti di virulenza non classici — la capacità di interagire con altri patogeni e con l’ospite in modi che promuovono la progressione della malattia. Questo spiega perché, nella pratica clinica, la riduzione di T. denticola si accompagna spesso a un miglioramento clinico che supera il peso numerico del singolo batterio.
Holt e Ebersole lo avevano anticipato nel 2005 su Periodontology 2000: il complesso rosso è un consorzio, e va trattato come tale. Non si elimina un membro alla volta. Si distrugge l’habitat.
Curiosità: analogie tra T. Pallidum (Sifilide) e T. Denticola
Entrambi appartengono al phylum Spirochaetota, famiglia Treponemataceae, genere Treponema. La vicinanza filogenetica implica un’architettura cellulare condivisa, meccanismi di motilità analoghi, e strategie patogenetiche convergenti.
La morfologia è identica nella forma: corpo elicoidale, 6–20 µm, con flagelli periplasmici che conferiscono la caratteristica motilità a cavatappi. È una motilità attiva anche in ambienti viscosi — tessuto connettivo, matrice extracellulare — che distingue le spirochete dalla maggior parte dei batteri parodontali.
Evasione immunitaria
T. pallidum è il maestro dell’evasione: superficie esterna quasi priva di proteine transmembrana esposte, scarsa immunogenicità, capacità di persistere per decenni. T. denticola utilizza strategie simili — degrada le immunoglobuline IgG e IgA attraverso proteasi specifiche, inibisce la chemiotassi dei neutrofili, sopravvive intracellularmente nei fibroblasti.
Produzione di proteasi
La dentilisina di T. denticola — una proteasi a cisteina — ha attività citotossica diretta, degrada componenti della matrice extracellulare e attiva le MMP dell’ospite. T. pallidum esprime anch’esso proteasi che facilitano la disseminazione tissutale.
Riferimenti
Ecco la bibliografia corretta:
- Dashper SG, Seers CA, Tan KH, Reynolds EC. Virulence factors of the oral spirochete Treponema denticola. J Dent Res. 2011;90(6):691-703. DOI
- Ishihara K. Virulence factors of Treponema denticola. Periodontol 2000. 2010;54(1):117-35. DOI
- Sela MN. Role of Treponema denticola in periodontal diseases. Crit Rev Oral Biol Med. 2001;12(5):399-413. DOI
- Holt SC, Ebersole JL. Porphyromonas gingivalis, Treponema denticola, and Tannerella forsythia: the “red complex”. Periodontol 2000. 2005;38:72-122. DOI
- Darveau RP. Periodontitis: a polymicrobial disruption of host homeostasis. Nat Rev Microbiol. 2010;8(7):481-90. DOI
- Zhu Y, Dashper SG, Chen YY, Crawford S, Slakeski N, Reynolds EC. Porphyromonas gingivalis and Treponema denticola synergistic polymicrobial biofilm development. PLoS One. 2013;8(8):e71727. DOI
- Kin LX, Butler CA, Slakeski N, Hoffmann B, Dashper SG, Reynolds EC. Metabolic cooperativity between Porphyromonas gingivalis and Treponema denticola. J Oral Microbiol. 2020;12(1):1808750. DOI
- Kurniyati K, Chang Y, Liu J, Li C. Identification and characterization of the alternative σ28 factor in Treponema denticola. J Bacteriol. 2022;204(9):e0024822. DOI
- Kokubu E, Kikuchi Y, Okamoto-Shibayama K, Nakamura S, Ishihara K. Crawling motility of Treponema denticola modulated by outer sheath protein. Microbiol Immunol. 2021;65(12):551-558. DOI
- Sano Y, Okamoto-Shibayama K, Tanaka K, Ito R, Shintani S, Yakushiji M, Ishihara K. Dentilisin involvement in coaggregation between Treponema denticola and Tannerella forsythia. Anaerobe. 2014;30:45-50. DOI
- Pisani F, Pisani V, Arcangeli F, Harding A, Singhrao SK. Treponema denticola has the potential to cause neurodegeneration in the midbrain via the periodontal route of infection—Narrative review. Int J Environ Res Public Health. 2023;20(11):6049. DOI
- Mahendrarajan V, Lazarus HPS, Muthukaliannan GK, Varghese S, Easwaran N. Membrane vesicles from Red Complex bacteria: key players in oral pathogenesis, immune disruption, systemic diseases, and therapeutic insights. Front Oral Health. 2025;6:1607931. DOI
Domande frequenti
- Cos'è il Treponema denticola?
- È una spirocheta Gram-negativa, anaerobia obbligata, membro del complesso rosso di Socransky. Vive nel solco gengivale profondo ed è fortemente associata alla parodontite cronica.
- Perché Treponema denticola è pericoloso per le gengive?
- Possiede flagelli periplasmatici che gli permettono di penetrare i tessuti, una proteasi chiamata dentilisina che degrada proteine dell'ospite, e la capacità di eludere il sistema immunitario. Inoltre collabora con Porphyromonas gingivalis in modo sinergico.
- Treponema denticola può causare malattie fuori dalla bocca?
- Studi recenti lo associano a neurodegenerazione (Alzheimer), aterosclerosi e complicanze gravidiche. La sua capacità di invadere i tessuti e viaggiare lungo i nervi periferici lo rende un sospettato plausibile.
- Come si può contrastare Treponema denticola?
- Con l'igiene orale domiciliare accurata, la terapia parodontale professionale e il mantenimento regolare. Essendo anaerobio obbligato, la rimozione meccanica del biofilm subgengivale è il metodo più efficace per ridurne la carica.
Referenze
- https://doi.org/10.1177/0022034510385242
- https://doi.org/10.1111/j.1600-0757.2009.00345.x
- https://doi.org/10.1177/10454411010120050301
- https://doi.org/10.1111/j.1600-0757.2005.00113.x
- https://doi.org/10.1038/nrmicro2337
- https://doi.org/10.1371/journal.pone.0071727
- https://doi.org/10.1080/20002297.2020.1808750
- https://doi.org/10.1128/jb.00248-22
- https://doi.org/10.1111/1348-0421.12940
Cerchi uno specialista?
Parodontologia a Frosinone →Diagnosi e trattamento della parodontite nello Studio Denti Più
Hai bisogno di un parere?
Prenota una visita nello studio del Dr. Bruschi a Frosinone. Prima visita con diagnosi completa e piano di trattamento personalizzato.
Resta aggiornato
Nuovi articoli su parodontologia, implantologia e chirurgia orale — nella tua casella email.
Commenti
Caricamento commenti...
Lascia un commento