La radiografia del Medico Odontoiatra che può salvarti le ossa: come l'AI trasforma l'OPT in uno screening dell'osteoporosi
Read in English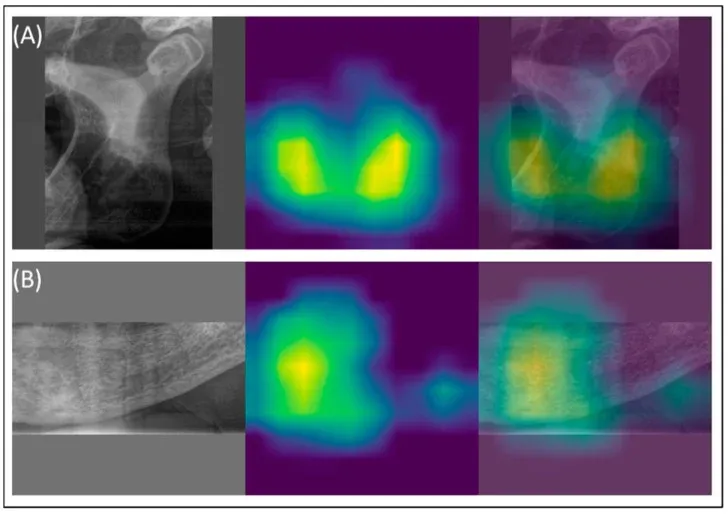
In breve — Due meta-analisi (2024–2025) dimostrano che l’AI può rilevare l’osteoporosi sull’ortopantomografia con sensibilità pooled dell’88%, contro il 35% della valutazione manuale. Lo studio del dentista — già il punto di accesso sanitario più frequentato — potrebbe diventare una prima linea di screening osseo senza costi aggiuntivi per il paziente.
Summary (EN) — Two meta-analyses (2024–2025) show that AI can detect osteoporosis from dental panoramic X-rays with pooled sensitivity of 88%, versus 35% for manual assessment. The dental office — already the most frequently visited healthcare touchpoint — could become a first-line bone screening point at near-zero extra cost.
Il paradosso dei 500 milioni
Cinquecento milioni di persone nel mondo vivono con l’osteoporosi. La maggioranza non lo sa. Non ha una diagnosi.
Non perché gli esami non esistano. Non perché i medici non siano incompetenti. Ma perché l’osteoporosi è una malattia insidiosa e silenziosa: non brucia, non gonfia, non dà febbre. Si manifesta solo quando qualcosa si rompe — una vertebra che cede sotto il peso di una borsa della spesa, un femore che si frattura con una caduta banale. A quel punto il danno è già avanzato, e il trattamento lavora in affanno.
Ogni tre secondi nel mondo si verifica una frattura da fragilità ossea correlata all’osteoporosi. In Europa, una donna su tre e un uomo su cinque sopra i cinquant’anni subirà almeno una frattura osteoporotica nel corso della vita. Eppure la MOC (o DEXA, Dual Energy X-ray Absorptiometry) — l’esame radiologico gold standard per misurare la densità minerale ossea — viene troppo spesso prescritta spesso solo dopo la prima frattura, quando sarebbe stato meglio agire anni prima — sia per intervenire con farmaci efficaci come bifosfonati e denosumab, sia per monitorare la risposta terapeutica nel tempo.
La domanda è sorge spontanea: esiste un modo semplice per intercettare questa malattia prima che si faccia sentire?
La risposta, emersa da due meta-analisi pubblicate tra il 2024 e il 2025, arriva da un posto inaspettato: lo studio del tuo medico odontoiatra.
Quella radiografia che fai (o richiedi) di routine
L’ortopantomografia — OPT o OPG, comunemente chiamata “panoramica” — è la radiografia esegue di routine negli studi odontoiatrici ogni uno o due anni. In un’unica immagine mostra tutti i denti, le ossa mascellari e mandibolari, i seni paranasali, le articolazioni temporo-mandibolari. È uno degli esami più comuni in medicina: in Italia si eseguono milioni di OPT ogni anno, a un costo compreso tra 30 e 70 euro.
Quello che la maggior parte dei pazienti non sa è che in quell’immagine è visibile molto più dei denti.
Il bordo inferiore della mandibola — la cosiddetta cortical plate o corticale mandibolare inferiore — riflette la salute ossea dell’intero scheletro. L’osso mandibolare risponde alle stesse variazioni ormonali, nutrizionali e metaboliche che condizionano la colonna vertebrale e il femore. Quando la densità ossea sistemica diminuisce, diminuisce anche lo spessore e la regolarità della corticale mandibolare.
I radiologi lo sanno da decenni. Già negli anni ‘90 erano stati sviluppati indici morfometrici specifici — il Mandibular Cortical Index (MCI), la Mandibular Cortical Width (MCW), il Panoramic Mandibular Index (PMI) — per valutare visivamente questi parametri sull’OPT e stimare il rischio di osteoporosi.
Il problema era la precisione.
Box scientifico — Il limite dell’occhio umano
Una meta-analisi del 2019 pubblicata su Dentomaxillofacial Radiology (Kinalski et al., PMID 31596133, 33 studi, 5.266 donne) ha misurato le performance del Mandibular Cortical Index valutato manualmente da radiologi esperti:
- Sensibilità per l’osteoporosi: 35%
- Specificità: 88%
Tradotto: su 100 donne con osteoporosi, l’occhio umano ne identificava correttamente solo 35. Le altre 65 venivano perse.
Un’alta specificità significa pochi falsi positivi — ma una sensibilità del 35% è troppo bassa per uno strumento di screening.
Entra l’intelligenza artificiale
Negli ultimi sei anni, decine di gruppi di ricerca in tutto il mondo hanno addestrato algoritmi di deep learning — reti neurali convoluzionali (CNN) nelle varianti ResNet, EfficientNet, VGG-16, GoogLeNet — ad analizzare le OPT e classificare automaticamente il rischio di osteoporosi, confrontando i risultati con la DXA come gold standard.
I risultati hanno sorpreso anche i ricercatori.
Nel 2019, un gruppo coreano (Lee et al., Dentomaxillofacial Radiology, PMID 30004241, 1.268 pazienti) pubblicò uno studio con una rete DCNN multi-colonna che raggiungeva un’AUC di 0,9987 — praticamente la perfezione diagnostica in condizioni controllate. Un risultato straordinario, ma su un singolo dataset.
Poi sono arrivate le meta-analisi, che aggregano i dati di decine di studi e producono stime più robuste e generalizzabili.
Box scientifico — Le due meta-analisi chiave
Ghasemi et al. (2025) — Journal of Dentistry, 24 studi inclusi
- Sensibilità pooled: 87,9%
- Specificità pooled: 81,9%
- Diagnostic Odds Ratio: 32,99
Khadivi et al. (2024) — Osteoporosis International, 22 studi inclusi
- DCNN: Sensibilità 87%, Specificità 92%
- Algoritmi convenzionali: Sens. 82%, Spec. 96%
Entrambe le meta-analisi confrontano i risultati AI con la DXA come gold standard.
Dal 35% dell’occhio umano all’88% dell’AI: più del doppio dell’efficacia diagnostica, sullo stesso esame, senza costi aggiuntivi per il paziente.
La specificità del 92% è particolarmente rilevante in un contesto di screening: significa che il sistema genera pochi falsi positivi, evitando di allertare inutilmente pazienti sani e di sovraccaricare il sistema con rinvii non necessari alla MOC.
Come “vede” l’AI — e dove guarda
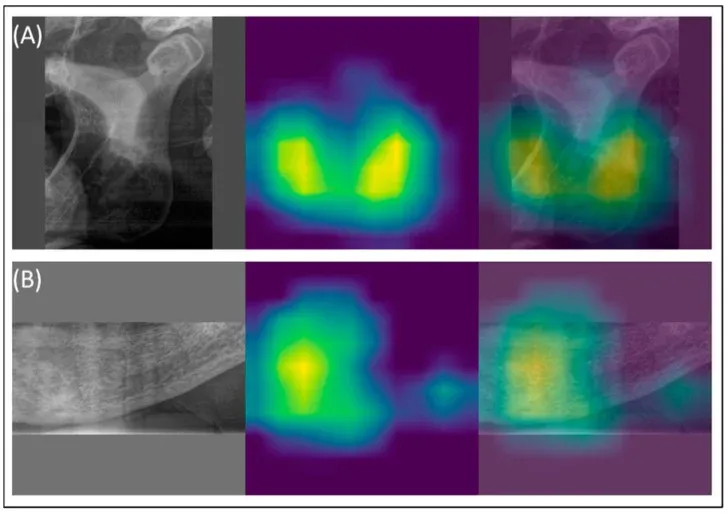
Uno degli aspetti più affascinanti di questa ricerca riguarda il meccanismo di funzionamento dei modelli. Grazie a tecniche di visualizzazione chiamate GradCAM (Gradient-weighted Class Activation Mapping), è possibile vedere letteralmente su quali zone dell’immagine si concentra l’attenzione della rete neurale quando classifica un caso come osteoporotico.
La risposta è precisa: il bordo inferiore della mandibola e il forame mentale (il foro attraverso cui passa il nervo mentoniero). Esattamente le stesse regioni anatomiche che un radiologo esperto esaminerebbe.
L’AI non ha imparato una scorciatoia statistica arbitraria. Ha imparato la stessa metodica che i clinici conoscono da decenni — solo con una velocità e una consistenza che l’occhio umano non può eguagliare in modo continuativo e sistematico.
Uno studio del gruppo della Charité di Berlino (Gaudin et al., 2024, Diagnostics, PMID 39451621) ha proposto un approccio ibrido: YOLOv8 per identificare automaticamente le regioni di interesse nell’immagine, poi EfficientNet per la classificazione. Risultato: sensibilità 83%, AUC 0,76. Non il valore più alto in assoluto, ma ottenuto con un rigore metodologico esplicito — inclusa la validazione esterna — che molti studi precedenti non garantivano.
Lo sapevi che — Il dato italiano
Nel 2025, un team italiano ha pubblicato su Journal of Clinical Medicine (Fanelli et al., PMID 40648835, università di Foggia e Parma, con validazione esterna) il primo studio con validazione esterna su dataset italiano.
Il modello ResNet-50, addestrato su 245 OPT di donne in post-menopausa e validato esternamente su 56 casi di Parma, ha raggiunto:
- Sensibilità: 90,5%
- AUC: 0,786
Alta sensibilità significa pochi casi di osteoporosi mancati — la qualità più importante per uno strumento di primo screening.
Il dentista come sentinella sistemica
C’è un dato epidemiologico che raramente entra nel dibattito clinico, ma che cambia completamente la prospettiva.
Negli Stati Uniti, secondo l’American Dental Association, il 65% degli adulti visita il dentista almeno una volta all’anno. Solo il 43% visita un medico di base con la stessa frequenza. I dati europei (Eurobarometer 2022) mostrano una media di 1,5 visite dentistiche annue per cittadino UE.
Lo studio dentistico è già, de facto, il punto di accesso più capillare al sistema sanitario — più del medico di medicina generale. Ogni anno milioni di persone entrano in quello studio, vengono sottoposte a una OPT di routine, e ne escono con informazioni cliniche che si fermano ai denti. Già durante la recente pandemia, gli studi dentistici sono diventati degli “HUB” per informazioni e prescrizioni sanitarie di pazienti bisognosi quando gli MMG non erano rapidamente disponibili. Non è un caso: l’odontoiatra intercetta segnali di malattie sistemiche — dall’osteoporosi al diabete — prima ancora del medico curante.
Integrare un modulo AI di analisi ossea nell’OPT già eseguita per altri motivi ha un costo marginale quasi nullo per il paziente. Non aggiunge radiazioni (l’OPT è già parte del percorso odontoiatrico), non richiede un secondo appuntamento, non impone un esame invasivo. Richiede un algoritmo e un flusso di lavoro.
Certo poi ci si mette, ovviamente, al burocrazia a complicare le cose: devi rispettare le normative sull’uso dell’intelligenza artificiale. E i colleghi, stufi di tante norme inutili, magari rinunciano a questi preziosi strumenti.
In termini di costo-efficacia: la MOC costa da tre a otto volte più di una radiografia panoramica. E richiede un’apparecchiatura dedicata, personale appositamente formato, e una prescrizione medica.
Per i professionisti — Il confronto degli indici
Confronto strutturato tra metodi di valutazione dell’OPT per screening osteoporosi:
Metodo Sensibilità Specificità Note MCI manuale 35% 88% Meta-analisi Kinalski 2019, 5.266 donne MCW ≤3 mm 42–60% 82–90% Buona specificità, bassa sensibilità MCI manuale + FRAX >15% Alta ~95% Combinazione ottimale pre-AI AI su OPT (pooled) 87–88% 82–95% Meta-analisi 2024–2025 MCI + densità alveolare (AI) — — AUC validazione esterna 0,97–1,00 (Okubo 2025) Il valore aggiunto dell’AI è quantificabile: non è un miglioramento marginale, è un salto di categoria nella sensibilità diagnostica.
Il limite attuale — e perché è importante dirlo
La ricerca è solida. Ma l’onestà intellettuale impone di dire anche dove siamo davvero.
La revisione sistematica più recente sull’argomento — Querrer et al., pubblicata su Dentomaxillofacial Radiology nel 2026 (PMID 40580938), 13 studi analizzati — ha evidenziato una lacuna critica: nessuno degli studi analizzati ha integrato questi modelli in uno studio dentistico reale. Tutti i risultati provengono da dataset retrospettivi, in condizioni sperimentali controllate.
Il gruppo della Charité ha sollevato un altro problema: molti dei risultati più ottimistici in letteratura (AUC >0,99) riflettono bias metodologici — selezione non bilanciata dei pazienti, mancanza di validazione esterna, confronto tra gruppi troppo distanti (pazienti giovani sani vs anziani osteoporotici). Quando si applica un rigore metodologico più severo, le performance calano — restando comunque clinicamente rilevanti, ma molto più lontane dalla “perfezione”.
La tecnologia è pronta. Il rigore scientifico è in corso di consolidamento. Manca il terzo elemento: il ponte tra laboratorio e studio dentistico. Interfacce accessibili, flussi di lavoro integrati nei software di gestione, protocolli di rinvio allo specialista, formazione dei clinici.
È questa la frontiera su cui il settore sta lavorando — e su cui nei prossimi anni vedremo i primi risultati reali.
Conclusione
L’ortopantomografia è uno degli esami medici più comuni al mondo. Per decenni ha fatto un solo lavoro: mostrarci i denti e le ossa dello splancnocranio. Oggi sappiamo che in quell’immagine c’è molto di più.
L’intelligenza artificiale ha trasformato una valutazione manuale con sensibilità del 35% in uno strumento di screening con sensibilità pooled dell’88% — su dati aggregati di decine di studi e decine di migliaia di pazienti. Non è fantascienza: è letteratura pubblicata su Osteoporosis International, Journal of Dentistry, Scientific Reports.
Il passo successivo non è tecnologico. È organizzativo: integrare questo strumento nella pratica clinica quotidiana, formare i dentisti a riconoscere i segnali di allarme osseo, costruire protocolli di rinvio tra studio dentistico e specialista in osteoporosi.
Quando quel passo sarà compiuto, la visita dal dentista non sarà più solo un controllo dei denti. Sarà anche — finalmente — una prima linea della salute delle ossa.
Domande Frequenti
L’OPT può sostituire la DXA?
No. L’OPT con AI è uno strumento di screening di primo livello — identifica i pazienti a rischio da indirizzare alla DXA per la diagnosi definitiva. Non la sostituisce.
Il mio dentista può già farlo?
Nella pratica clinica routinaria italiana, no. I modelli AI per l’analisi ossea dell’OPT non sono ancora integrati nei software odontoiatrici commerciali. Alcuni centri universitari potrebbero averli in fase sperimentale.
Cosa posso fare adesso?
Se hai più di 50 anni, sei in menopausa, hai già avuto una frattura o hai familiari con osteoporosi, parla con il tuo medico di base della possibilità di eseguire una DXA. Non aspettare che sia un algoritmo a dirti che c’è un problema.
Perché la mandibola riflette la salute ossea sistemica?
L’osso mandibolare risponde alle stesse variazioni ormonali, metaboliche e nutrizionali che condizionano colonna vertebrale e femore. La perdita di estrogeni in menopausa, la carenza di vitamina D, l’iperattività osteoclastica — tutti questi meccanismi agiscono sull’intero scheletro, mandibola inclusa.
Fonti
- Ghasemi et al. (2025) — Journal of Dentistry — PMID 40010536
- Khadivi et al. (2024) — Osteoporosis International — PMID 39177815
- Fanelli et al. (2025) — Journal of Clinical Medicine — PMID 40648835
- Querrer et al. (2026) — Dentomaxillofacial Radiology — PMID 40580938
- Kinalski et al. (2019) — Dentomaxillofacial Radiology — PMID 31596133
- Gaudin et al. (2024) — Diagnostics — PMID 39451621
- Turosz et al. (2023) — Dentomaxillofacial Radiology — PMID 37665008
- Lee et al. (2019) — Dentomaxillofacial Radiology — PMID 30004241
Domande frequenti
- L'OPT può sostituire la DXA?
- No. L'OPT con AI è uno strumento di screening di primo livello — identifica i pazienti a rischio da indirizzare alla DXA per la diagnosi definitiva. Non la sostituisce.
- Il mio dentista può già farlo?
- Nella pratica clinica routinaria italiana, no. I modelli AI per l'analisi ossea dell'OPT non sono ancora integrati nei software odontoiatrici commerciali. Alcuni centri universitari potrebbero averli in fase sperimentale.
- Cosa posso fare adesso?
- Se hai più di 50 anni, sei in menopausa, hai avuto fratture o hai familiari con osteoporosi, parla con il tuo medico di base della possibilità di eseguire una DXA.
- Perché la mandibola riflette la salute ossea sistemica?
- L'osso mandibolare risponde alle stesse variazioni ormonali, metaboliche e nutrizionali che condizionano colonna vertebrale e femore. Perdita di estrogeni, carenza di vitamina D e iperattività osteoclastica agiscono sull'intero scheletro, mandibola inclusa.
Referenze
- https://pubmed.ncbi.nlm.nih.gov/40010536/
- https://pubmed.ncbi.nlm.nih.gov/39177815/
- https://pubmed.ncbi.nlm.nih.gov/40648835/
- https://pubmed.ncbi.nlm.nih.gov/40580938/
- https://pubmed.ncbi.nlm.nih.gov/31596133/
- https://pubmed.ncbi.nlm.nih.gov/39451621/
- https://pubmed.ncbi.nlm.nih.gov/37665008/
- https://pubmed.ncbi.nlm.nih.gov/30004241/
Cerchi uno specialista?
Innesto Osseo a Frosinone →Tipi di innesto, tecniche e indicazioni per ricostruire l'osso perduto
Hai bisogno di un parere?
Prenota una visita nello studio del Dr. Bruschi a Frosinone. Prima visita con diagnosi completa e piano di trattamento personalizzato.
Resta aggiornato
Nuovi articoli su parodontologia, implantologia e chirurgia orale — nella tua casella email.
Commenti
Caricamento commenti...
Lascia un commento