L'asse menopausa-gengive che la medicina sta riscoprendo
Read in English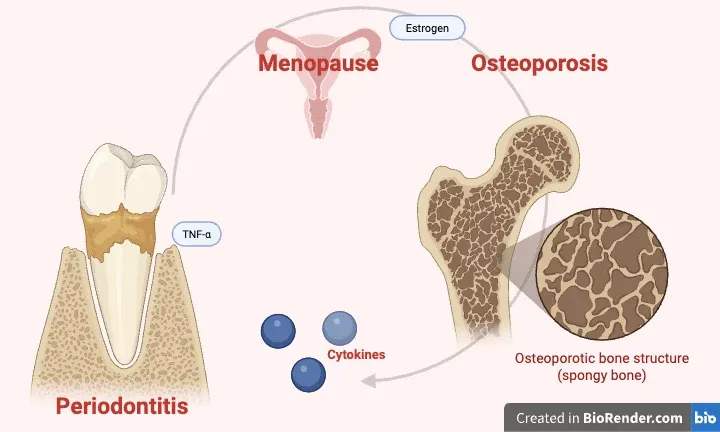
In breve — Una meta-analisi 2023 su 19.611 pazienti dimostra che le donne in post-menopausa con osteoporosi hanno parodontite più grave (+0,89 mm di perdita di attacco clinico) rispetto a quelle senza osteoporosi. Uno studio coreano su 2.573 donne identifica nei primi 4 anni dopo la menopausa la finestra critica: il rischio di parodontite raddoppia. Le due malattie condividono la stessa biologia infiammatoria.
Summary (EN) — A 2023 meta-analysis on 19,611 patients shows postmenopausal women with osteoporosis have more severe periodontitis (+0.89 mm clinical attachment loss) than those without. A Korean study on 2,573 women identifies the first four years after menopause as the critical window: periodontal disease risk doubles. The two conditions share the same inflammatory biology.
Due malattie, una sola biologia
Pensa a quella persona che conosci che ha scoperto di avere l’osteoporosi, magari dopo una brutta frattura o un crollo vertebrale.
Ora pensa a chi ha problemi di gengive. Nella tua mente, probabilmente, sono due persone diverse, con percorsi di cura diversi.
E invece potrebbe essere la stessa persona.
La correlazione tra osteoporosi e malattia parodontale è uno dei capitoli più fertili — e più sottovalutati — della medicina contemporanea. Fertili perché i dati si accumulano rapidamente, con numeri che ormai superano le decine di migliaia di pazienti. Sottovalutati perché il confine tra medicina e odontoiatria, storicamente separato in modo netto, rallenta la diffusione di queste evidenze verso chi ne avrebbe più bisogno: i pazienti stessi.
Questo articolo è un tentativo di abbattere quel confine, come già fatto con altri — dati alla mano.
Il numero che cambia la prospettiva
Nel 2023, una meta-analisi pubblicata su Heliyon (Qi et al., PMID 37920517) ha aggregato i dati di 28 studi osservazionali, per un totale di 19.611 pazienti. L’obiettivo era rispondere a una domanda precisa: le donne in post-menopausa con osteoporosi hanno condizioni parodontali sovrapponibili o peggiori rispetto a quelle che non ne sono affette?
Potrebbe sorprenderti, ma la risposta è che la parodontite è più grave nel gruppo con osteoporosi — e non di poco.
Rispetto alle donne senza osteoporosi, quelle con diagnosi di osteoporosi mostravano:
- +0,89 mm di perdita di attacco clinico (CAL) — la misura diretta del danno al tessuto parodontale
- +0,27 mm di profondità di sondaggio (PD) — indice di infiammazione attiva
- +0,28 mm di recessione gengivale (GR)
- +12,71% di sanguinamento al sondaggio (BOP) — segnale classico di infiammazione gengivale
- densità minerale ossea (BMD) significativamente inferiore anche nei siti dentali
Singolarmente, qualcuno di questi valori potrebbe sembrare una differenza numerica astratta. Ma 0,89 mm in più di perdita di attacco clinico, su una popolazione di quasi ventimila persone, rappresenta una distanza clinicamente rilevante: in molte pazienti, potrebbe voler dire la differenza tra una parodontite lieve e una moderata, tra un dente che si salva e uno con prognosi infausta.
Box scientifico — Cosa misuriamo quando misuriamo la parodontite
La perdita di attacco clinico (CAL) è la misura principale della progressione della malattia parodontale. Indica di quanti millimetri il tessuto che ancora “tiene” il dente si è distaccato dalla superficie radicolare. Un CAL ≥3 mm è soglia clinica di parodontite secondo la classificazione 2017; ≥5 mm indica una forma moderata-grave.
Il sanguinamento al sondaggio (BOP, Bleeding On Probing) è la risposta del tessuto gengivale alla sonda diagnostica: quando sanguina, c’è infiammazione attiva. Un BOP >25% è associato a progressione del danno parodontale.
La profondità di sondaggio (PD) misura la profondità della tasca gengivale: oltre i 4 mm, l’igiene domiciliare diventa inefficace e l’infiammazione tende a cronicizzarsi.
La finestra critica: i quattro anni dopo la menopausa
Se la meta-analisi fornisce la dimensione del fenomeno, uno studio coreano pubblicato su PLoS ONE (Lee Y., 2022, PMID 35298563) ne illumina la dinamica temporale — e il risultato è forse ancora più rilevante dal punto di vista clinico.
Lo studio ha analizzato i dati del Korea National Health and Nutrition Examination Survey (KNHANES) su 2.573 donne in menopausa, stratificando il campione per anni trascorsi dall’ultima mestruazione.
Il rischio complessivo di malattia parodontale nelle donne con osteoporosi era già significativamente elevato: OR = 1,25 (95% CI: 1,00–1,56). Ma quando si analizzavano separatamente le donne nei primi quattro anni dalla menopausa, il rischio quasi raddoppiava:
OR* = 2,08 (95% CI: 1,15–3,77)
*L’Odds Ratio (OR), o rapporto di probabilità, è una misura statistica che quantifica la forza dell’associazione tra due eventi.
Tradotto in termini clinici: una donna con osteoporosi che ha superato la menopausa da meno di quattro anni ha il doppio delle probabilità di sviluppare malattia parodontale rispetto a una donna senza osteoporosi nella stessa fase.
Questo dato ha un’implicazione pratica immediata: la transizione menopausale è la finestra temporale in cui l’interazione tra le due patologie è più intensa — e quindi il momento in cui la prevenzione e la diagnosi precoce hanno il massimo potenziale di efficacia.
Lo sapevi che — Il fattore genere
Uno studio epidemiologico taiwanese condotto sul database nazionale (Lin et al., 2015, Medicine, PMID 25700325) ha analizzato la relazione tra parodontite e osteoporosi separatamente per uomini e donne.
Risultato: nelle donne, il rischio era significativamente elevato — OR 1,96 (95% CI: 1,17–3,26). Negli uomini, l’associazione non era statisticamente significativa.
Questo non significa che gli uomini siano immuni: significa che nelle donne il sistema ormonale — e in particolare il calo degli estrogeni — è un amplificatore potente del rischio condiviso tra le due malattie.
Perché succede: la biologia condivisa
La correlazione tra osteoporosi e parodontite non è una coincidenza statistica. Ha una spiegazione biologica precisa, che la ricerca degli ultimi anni ha progressivamente chiarito.
Entrambe le malattie nascono da uno squilibrio nel rimodellamento osseo: la bilancia tra osteoblasti (le cellule che costruiscono osso) e osteoclasti (quelle che lo demoliscono) pende verso la demolizione. Nell’osteoporosi, questo squilibrio è sistemico — riguarda tutto lo scheletro. Nella parodontite, è localizzato all’osso alveolare, quello che sostiene i denti. Le cause sono diverse, i meccanismi molecolari finali sono simili.
Il fulcro è l’infiammazione cronica.
Box scientifico — Le citochine che fanno il danno
Tre molecole infiammatorie giocano un ruolo centrale in entrambe le patologie:
- IL-1β (Interleuchina-1β): potente stimolatore dell’attività osteoclastica; elevata sia nel fluido crevicolare gengivale dei pazienti parodontitici che nel siero dei pazienti con osteoporosi.
- TNF-α (Tumor Necrosis Factor alfa): promuove il riassorbimento osseo e inibisce la formazione osteoblastica; in entrambe le patologie i livelli sierici sono cronicamente elevati.
- IL-6 (Interleuchina-6): regolatore chiave dell’asse RANK/RANKL/OPG che governa il turnover osseo; la sua iperproduzione accelera il riassorbimento sia alveolare che sistemico.
Fonte: Yu B, Wang CY, Periodontology 2000, 2022, PMID 35244945.
La parodontite non è solo una malattia locale della bocca. I batteri del biofilm sottogengivale e i mediatori infiammatori che producono entrano nel circolo sistemico — e quando lo fanno, alzano i livelli di questi stessi marcatori nel sangue. In un organismo già in stato infiammatorio cronico — come quello di una donna in menopausa con osteoporosi — questo contributo si somma a quello esistente, peggiorando entrambe le condizioni.
È questo il senso della relazione bidirezionale: l’osteoporosi aumenta la suscettibilità alla perdita di osso alveolare, e la parodontite non trattata alimenta l’infiammazione sistemica che a sua volta accelera il riassorbimento scheletrico. Le due malattie si nutrono reciprocamente.
Una review del 2026 firmata da Maria Contaldo (Università della Campania Luigi Vanvitelli, su Advances in Experimental Medicine and Biology — PMID 41225098) identifica nella disbiosi del microbiota orale — e di quello intestinale — un elemento critico in entrambe le patologie: la perturbazione dell’ecosistema microbico condiviso crea le condizioni per il mantenimento di uno stato infiammatorio cronico che non si risolve né a livello gengivale né a livello osseo sistemico.
Il ruolo degli estrogeni
Il calo degli estrogeni in menopausa non agisce solo sulle ossa. Agisce anche sulle gengive.
Gli estrogeni modulano la risposta immunitaria locale nel cavo orale, la composizione del microbiota, la densità dell’osso alveolare e l’attività della collagenasi — l’enzima che degrada il collagene dei tessuti di supporto del dente. Quando i livelli di estrogeni scendono bruscamente, come avviene nei primi anni dopo la menopausa, questi effetti protettivi si riducono contemporaneamente su tutti i fronti.
Una review pubblicata su Cureus nel 2025 (Jawed et al., PMID 40462880) ha analizzato sistematicamente il legame tra variazioni ormonali femminili e salute gengivale, confermando che il periodo di transizione menopausale rappresenta una fase di aumentata vulnerabilità del tessuto parodontale — indipendentemente dall’igiene orale e dallo stato di salute dentale preesistente.
Questo dato ha un’implicazione pratica spesso trascurata: una donna che inizia la menopausa dovrebbe discutere con il proprio dentista non solo di densità ossea, ma anche di salute gengivale — e viceversa. I due percorsi di prevenzione non dovrebbero essere paralleli e separati, ma integrati.
Lo sapevi che — I fattori di rischio condivisi
Osteoporosi e parodontite non condividono solo i meccanismi biologici. Condividono anche i fattori di rischio modificabili:
- Carenza di vitamina D: riduce la mineralizzazione ossea sistemica e aumenta la suscettibilità all’infiammazione parodontale.
- Fumo di sigaretta: accelera il riassorbimento osseo e compromette la vascolarizzazione gengivale, mascherando il sanguinamento (falsa sicurezza).
- Sedentarietà: riduce lo stimolo meccanico sull’osso, necessario per il mantenimento della massa ossea.
- Dieta povera di calcio e proteine: impoverisce sia la struttura ossea sistemica che quella alveolare.
Intervenire su questi fattori significa ridurre il rischio di entrambe le patologie contemporaneamente.
Cosa cambia nella pratica
La ricerca su questa correlazione non è ancora entrata pienamente nella pratica clinica quotidiana — né in quella medica né in quella odontoiatrica. Ma i dati disponibili giustificano già alcuni cambiamenti concreti nel modo in cui gestiamo questi pazienti.
Per il dentista. Una paziente in menopausa con diagnosi di osteoporosi è, per definizione, una paziente ad alto rischio parodontale. Merita un monitoraggio più frequente, una soglia di allerta più bassa, e un raccordo attivo con il medico di base o con il reumatologo — soprattutto in caso di terapia con bifosfonati o denosumab, che impatta direttamente anche sul piano implantare e parodontale. I parametri parodontali — CAL, BOP, PD — non sono solo dati odontoiatrici: in questo contesto diventano indicatori del rischio sistemico. È anche il caso in cui un’analisi AI dell’ortopantomografia può aggiungere un livello di screening osseo alla visita dentistica routinaria.
Per il medico. Un paziente con osteoporosi che non ha avuto una visita parodontale di controllo negli ultimi dodici mesi ha una lacuna nel suo percorso di prevenzione. Il rinvio al dentista — non solo per il controllo della carie, ma specificamente per la valutazione parodontale — dovrebbe far parte del piano terapeutico standard. È uno dei casi in cui l’odontoiatra può intercettare segnali sistemici che integrano la gestione della malattia di base.
Per il paziente. Se sei in menopausa e hai una diagnosi di osteoporosi, o anche solo una densità ossea ridotta, sappi che le tue gengive sono in una fase di maggiore vulnerabilità. Non aspettare il dolore o il sanguinamento per andare dal dentista: a quel punto l’infiammazione è già attiva da tempo.
Conclusione
Cinquant’anni fa, l’idea che le gengive e la colonna vertebrale o la testa del femore potessero “parlare” la stessa lingua biologica sarebbe sembrata speculativa. Oggi abbiamo 19.611 pazienti di una meta-analisi che lo confermano, studi su decine di migliaia di donne che identificano la finestra temporale critica, e una comprensione molecolare sufficientemente dettagliata da spiegare il perché.
La sfida ora non è scientifica. È organizzativa e culturale: abituarci a guardare la bocca come parte del corpo, e il corpo come sistema unico in cui gengive, ossa, ormoni e infiammazione si influenzano reciprocamente.
La prossima volta che vai dal dentista — o che ci mandi un paziente — tienilo a mente.
Domande Frequenti
Se ho l’osteoporosi, svilupperò sicuramente la parodontite?
No. L’associazione statistica non è determinismo clinico. Avere l’osteoporosi aumenta il rischio, ma non garantisce che la parodontite si sviluppi — soprattutto se l’igiene orale è buona e i controlli sono regolari.
Se curo la parodontite, migliora anche la mia osteoporosi?
I dati su questo fronte sono ancora preliminari. Alcuni studi suggeriscono che il trattamento della parodontite riduce i marker infiammatori sistemici — tra cui quelli legati al riassorbimento osseo — ma non esistono ancora trial clinici randomizzati che dimostrino un miglioramento diretto della densità minerale ossea a seguito della sola terapia parodontale.
La relazione vale anche per gli uomini?
L’evidenza più solida riguarda le donne in post-menopausa, per il ruolo amplificatore degli estrogeni. Negli uomini l’associazione esiste ma è meno studiata e statisticamente meno robusta. Non significa che non sia rilevante: significa che mancano ancora studi con campioni maschili adeguati.
Devo preoccuparmi se ho solo “le gengive che sanguinano”?
Il sanguinamento gengivale è sempre un segnale di infiammazione attiva. Non significa automaticamente parodontite grave, ma è sempre un motivo valido per una valutazione dal dentista. In un contesto di menopausa e ridotta densità ossea, merita attenzione ancora maggiore.
Fonti
- Qi J et al. (2023) — Heliyon — PMID 37920517 — meta-analisi, 28 studi, 19.611 pazienti
- Lee Y. (2022) — PLoS ONE — PMID 35298563 — KNHANES, 2.573 donne
- Yu B, Wang CY (2022) — Periodontology 2000 — PMID 35244945 — meccanismi infiammatori condivisi
- Contaldo M. (2026) — Adv Exp Med Biol — PMID 41225098 — relazione bidirezionale e disbiosi
- Lin TH et al. (2015) — Medicine — PMID 25700325 — coorte taiwanese, fattore genere
- Jawed STM et al. (2025) — Cureus — PMID 40462880 — variazioni ormonali e salute gengivale
Domande frequenti
- Se ho l'osteoporosi, svilupperò sicuramente la parodontite?
- No. L'associazione statistica non è determinismo clinico. Avere l'osteoporosi aumenta il rischio, ma non garantisce che la parodontite si sviluppi — soprattutto se l'igiene orale è buona e i controlli sono regolari.
- Se curo la parodontite, migliora anche la mia osteoporosi?
- I dati su questo fronte sono ancora preliminari. Alcuni studi suggeriscono che il trattamento della parodontite riduce i marker infiammatori sistemici — tra cui quelli legati al riassorbimento osseo — ma non esistono ancora trial randomizzati che dimostrino un miglioramento diretto della densità minerale ossea a seguito della sola terapia parodontale.
- La relazione vale anche per gli uomini?
- L'evidenza più solida riguarda le donne in post-menopausa, per il ruolo amplificatore degli estrogeni. Negli uomini l'associazione esiste ma è meno studiata e statisticamente meno robusta. Non significa che non sia rilevante: significa che mancano ancora studi con campioni maschili adeguati.
- Devo preoccuparmi se ho solo le gengive che sanguinano?
- Il sanguinamento gengivale è sempre un segnale di infiammazione attiva. Non significa automaticamente parodontite grave, ma è un motivo valido per una valutazione dal dentista. In un contesto di menopausa e ridotta densità ossea, merita attenzione ancora maggiore.
Referenze
Cerchi uno specialista?
Parodontologia a Frosinone →Diagnosi e trattamento della parodontite nello Studio Denti Più
Hai bisogno di un parere?
Prenota una visita nello studio del Dr. Bruschi a Frosinone. Prima visita con diagnosi completa e piano di trattamento personalizzato.
Resta aggiornato
Nuovi articoli su parodontologia, implantologia e chirurgia orale — nella tua casella email.
Commenti
Caricamento commenti...
Lascia un commento